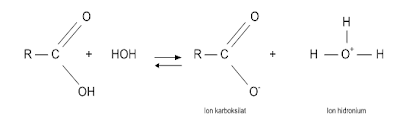
Asam karboksilat mengurai dalam air menghasilkan anion karboksilat dan ion hidronium.
Keasaman asam karboksilat :
• ditentukan oleh mudahnya gugus karboksil melepaskan ion hidrogen
• bersifat asam lemah
Keasaman diukur secara kuantiatif dengan
tetapan keasaman atau ionisasi, Ka . nilai Ka suatu asam
dinyatakan :
• masih jauh lebih asam dari senyawa-senyawa organik lainnya
• Kekuatan asam karboksilat sangat dipengaruhi oleh substituen yang terikat pada gugus alkil asam
karboksilat
• Substituen yang dapat menstabilkan ion karboksilat akan meningkatkan keasaman asam karboksilat

daftar gugus dalam urutan daya menarik elektronnya :
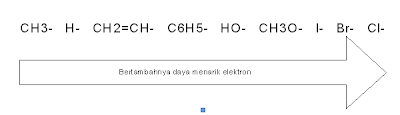
• Substituen yang menurunkan kestabilan ion karboksilat akan menurunkan keasaman asam karboksilat
• Asam kloroasetat >>> dari asam asetat, sebab asam kloro asetat memiliki satu gugus penarik elektron
yaitu klor .
• Klor (Cl) akan menarik elektron melalui efek induksi sehingga mengurangi kerapatan elektron dari karbon
α, akibatnya muatan negatif gugus karboksilat sebagian tersebar oleh muatan δ+ di dekatnya.
• Pengaruh efek induksi makin berkurang dengan makin banyaknya atom yang berada diantara gugus
karboksil dan gugus penarik elektron.
Sumber :
ml.scribd.com/doc/50534810/ASAM-KARBOKSILAT-1
Pertanyaan :
Pada artikel diatas disebutkan bahwa "Pengaruh efek induksi makin berkurang dengan makin banyaknya atom yang berada diantara gugus karboksil dan gugus penarik elektron". yang saya tanyakan , bagaimana caranya agar pengaruh efek induksi itu tidak berkurang meskipun dengan jumlah atom yang semakin banyak diantara gugus karboksil dan gugus penarik elektron tersebut.






Assalamualaikum.
BalasHapusnama: mahirullah
nim: a1c111055
nama blog: mahirullah.wordpress.com
tolong dioment uga y blog ku..
seperti yang telah dijelaskan beberapa minggu lalu..
sebagai akibat gaya van der wals pada H dari rantai panjang terhadap O dari karboksil, rantai panjang tersebut mengelilingi/menutupi bagian karboksilat yang reaktif sehingga mengakibatkan air tidak dapat membentuk ikatan hidrogen terhadap O dari karboksil..
sehingga dapat saya simpulkan bahwa penutupan tersebut mengakibatkan kestabilan asam karboksilat berkurang dan tingkat keasaman pun ikut berkurang..
jadi hal mungkin dapat dilakukan adalah memberikan katalis yang dapat membuka rantai panjang tersebut agar tidak menutupi gugus karboksil, dan hal itu dapat dilakukan jika gaya van der wals dari arilnya terhadap karboksil tersebut harus dipisahkan..
sekian terima kasih..
Posisi gugus COOH dan atom penginduksi menentukan besarnya efek induksi yang diberikan.jadi saya rasa tidak memungkinkan untuk membuat efek induksi yang besar dengan jarak yang besar pula,
BalasHapusEfek induksi terpancar melalui ikatan, dengan menggeser elektron ikatan ke arah atom elektronegatif atau menjauhi atom elektropositif. Ingat bahwa gugus penarik elektron meningkatkan keasaman, dan gugus pelepas elektron menurunkan keasaman.
BalasHapusKarena klorin lebih elektronegatif dibandingkan karbon, ikatan C-Cl terpolarisasi dengan klorin membawa muatan negatif parsial dan karbon positif parsial. Jadi elektron tertarik menjauhi ujung ion karboksilat ke arah klorin. Efek ini cenderung menyebarkan muata negatif pada atom yang lebih banyak dibandingkan pada ion asetat sendiri dan dengan demikian menstabilkan ion yang bersangkutan. Semakin banyak klorin, semakin besar efek induktif dan semakin besar kekuatan asam.
Jika klorin tersebut semakin menjauhi -COO- maka keasamannya semakin lemah karena ikatan yang terbentuk antara gugus penarik elektron juga semakin lemah seiring dengan semkin jauhnya klorin tersebut dengan gugus -COO-. Itulah sebabnya jika klorin tersebut semakin menjauhi -COO- maka keasamannya semakin lemah.
kemungkinan bisa trjadi jika penambahan clor